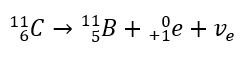สารเคมีรีเอเจนต์, รีเอเจนต์ pH, การวิเคราะห์เชิงคุณภาพ, การวิเคราะห์เชิงปริมาณ – นี่เป็นเพียงส่วนหนึ่งของคำศัพท์ที่เกี่ยวข้องกับเคมีวิเคราะห์ มีอะไรอีกบ้างที่ซ่อนอยู่ในสาขาเคมีนี้? คุณสามารถหาคำตอบสำหรับคำถามนี้ได้ในส่วนนี้!
สินค้า
วัตถุดิบเคมี
การดูแลส่วนบุคคลและการดูแลบ้าน
การก่อสร้างอาคาร

การขุดเจาะและการขุดอุโมงค์

กาวก่อสร้าง

ฉนวนท่อในท่อ

ฉนวนสายไฟและสายเคเบิล

ฉนวนโฟมสเปรย์

ท่อฉนวนสำเร็จรูป

ฝาครอบท่อ

พลาสเตอร์บอร์ดและสารเติมแต่งยิปซั่ม

พุกเคมี

ระบบฉนวน PU

ระบบสเปรย์ความร้อนและอะคูสติก

สารเติมแต่งคอนกรีตและมอร์ตาร์

สารเติมแต่งแอสฟัลต์

อุตสาหกรรมไม้

เครื่องปั้นดินเผา

แผงแซนวิช

แผ่นฉนวน

แอปพลิเคชั่นอื่นๆ

โอซีเอฟ (โฟมส่วนประกอบเดียว)
การขนส่ง
การทำความสะอาดและการซักล้าง
การป้องกันอัคคีภัย
กาวและวัสดุยาแนว
น้ำมันหล่อลื่นและของเหลวสำหรับงานโลหะ
พลังงานและทรัพยากร
พลาสติกและยาง
สารเคลือบและหมึก
สิ่งทอและหนัง
สเปรย์ฉนวนกันความร้อน
อุตสาหกรรมอาหาร
อุตสาหกรรมอิเล็กทรอนิกส์และไฟฟ้า
อุตสาหกรรมเฟอร์นิเจอร์
เคมีเกษตร
INCI ที่แนะนำสำหรับการใช้งานทางการเกษตร
เยื่อกระดาษและกระดาษ
ตัวอย่างคุณสมบัติของผลิตภัณฑ์
อินซีไอและแคส
สินค้าอุปโภคบริโภคและบรรจุภัณฑ์
สารลดแรงตึงผิว











































































































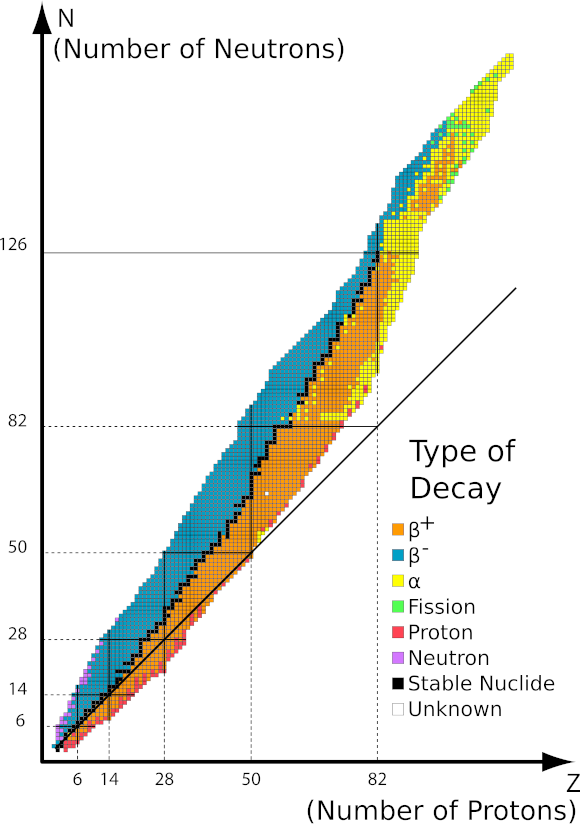
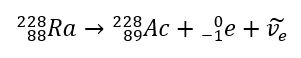 รังสีนี้มีลักษณะเป็นอนุภาคที่มีประจุลบซึ่งมีช่วงหลายโหลเซนติเมตรในอากาศและสามารถซึมผ่านได้มากกว่าเมื่อเทียบกับรังสีแอลฟา หยุดด้วยแผ่นอะลูมิเนียมที่มีความหนาประมาณ 3 ถึง 4 มม. การสลายตัวของเบต้าบวกเกิดขึ้นในลักษณะเดียวกัน แต่จะปล่อยอนุภาคโพซิตรอนและนิวตริโนของอิเล็กตรอนออกมา จำนวนโปรตอนในนิวเคลียสจะลดลงและธาตุที่ผ่านเข้าไปจะเปลี่ยนเป็นธาตุอื่นที่มีเลขอะตอมต่ำกว่า ดังตัวอย่าง
รังสีนี้มีลักษณะเป็นอนุภาคที่มีประจุลบซึ่งมีช่วงหลายโหลเซนติเมตรในอากาศและสามารถซึมผ่านได้มากกว่าเมื่อเทียบกับรังสีแอลฟา หยุดด้วยแผ่นอะลูมิเนียมที่มีความหนาประมาณ 3 ถึง 4 มม. การสลายตัวของเบต้าบวกเกิดขึ้นในลักษณะเดียวกัน แต่จะปล่อยอนุภาคโพซิตรอนและนิวตริโนของอิเล็กตรอนออกมา จำนวนโปรตอนในนิวเคลียสจะลดลงและธาตุที่ผ่านเข้าไปจะเปลี่ยนเป็นธาตุอื่นที่มีเลขอะตอมต่ำกว่า ดังตัวอย่าง