Хімічні реактиви, pH-реагенти, якісний аналіз, кількісний аналіз – це лише деякі терміни, пов’язані з аналітичною хімією. Що ще приховано в цій галузі хімії? Відповіді на це питання ви знайдете в цьому розділі!
Продукти
Хімічна сировина
Особиста гігієна та догляд вдома
Агрохімікати
Рекомендовані продукти
Рекомендований INCI для сільськогосподарського застосування
Будівництво

OCF (однокомпонентна піна)

Ізоляційна плита

Ізоляція з напилюваної піни

Ізоляція проводів і кабелів

Ізоляція труба в трубі

Інші програми

Анкери хімічні

Будівельна кераміка

Будівельні клеї

Буріння та проходка тунелів

Гіпсокартон і добавки до гіпсу

Деревообробна промисловість

Добавки для бетону та розчину

Добавки до асфальту

Кришки для труб

Попередньо ізольовані труби

Сендвіч панелі

Системи поліуретанової ізоляції

Теплові та акустичні системи розпилення
Електроніка та електротехнічна промисловість
Енергетика та ресурси
Клеї та герметики
Мастила та рідини для металообробки
Меблева промисловість
Напилювана ізоляція
Пластмаси та гуми
Покриття та чорнила
Профілактика пожеж
Текстиль та шкіра
Транспорт
Фармацевтика
Харчова промисловість
Целюлоза та папір
Приклади характеристик продукту
Чищення та прання
INCI та CAS
Споживчі товари

Рідкі мила

Засоби для виведення плям з тканини

Засоби для чищення та догляду за меблями

Засоби для чищення кухні

Засоби для чищення ванної кімнати

Засоби для миття вікон

Туалетні рідини

Засоби для миття посуду та лосьйони

Кондиціонери та концентрати для білизни

Миючі рідини та гелі

Багатоцільова продукція

Засоби для миття посуду































































































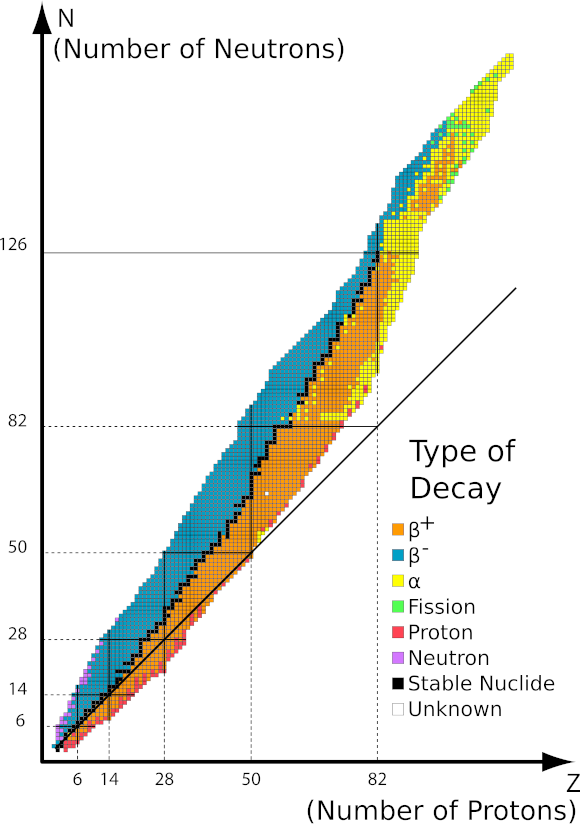
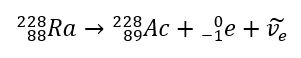 Це випромінювання характеризується негативно зарядженими частинками з радіусом дії в кілька десятків сантиметрів у повітрі та більшою проникністю порівняно з альфа-випромінюванням. Він закривається алюмінієвим листом товщиною приблизно від 3 до 4 мм. Бета-плюс розпад відбувається подібним чином, але він випромінює позитронні частинки та електронні нейтрино. Кількість протонів у ядрі зменшується, і елемент, який зазнає цього, перетворюється на інший з меншим атомним номером, як у прикладі:
Це випромінювання характеризується негативно зарядженими частинками з радіусом дії в кілька десятків сантиметрів у повітрі та більшою проникністю порівняно з альфа-випромінюванням. Він закривається алюмінієвим листом товщиною приблизно від 3 до 4 мм. Бета-плюс розпад відбувається подібним чином, але він випромінює позитронні частинки та електронні нейтрино. Кількість протонів у ядрі зменшується, і елемент, який зазнає цього, перетворюється на інший з меншим атомним номером, як у прикладі: