Reagentes químicos, reagentes de pH, análise qualitativa, análise quantitativa – estes são apenas alguns dos termos associados à química analítica. O que mais está escondido neste campo da química? Você pode encontrar as respostas para esta pergunta nesta seção!
Produtos
Matérias-primas químicas
Cuidados Pessoais e Cuidados Domiciliares
Adesivos e Selantes

Matérias-primas para produção de adesivos

Adesivos de espuma Rebond

Adesivos de grânulos de borracha

Adesivos e Primeres para Painéis Sanduíche

Adesivos para madeira

Adesivos para reforço de maciços rochosos

Adesivos para superfícies esportivas e recreativas

Adesivos universais

Impermeabilização

Poliureias

Aditivos
Agroquímicos

Produtos de proteção de plantas

Adjuvantes

Bioestimulantes

Fertilizantes Foliares

Fertilizantes a lanço
Produtos recomendados
INCI recomendado para aplicações agrícolas
Construção civil

Adesivos de construção

Aditivos para asfalto

Aditivos para concreto e argamassa

Cerâmica de construção

Industria madeireira

Isolamento Pipe-in-pipe

Isolamento de espuma em spray

Isolamento de fios e cabos

OCF (espuma de um componente)

Outras aplicações

Painéis sanduíche

Perfuração e tunelamento

Placas de gesso e aditivos de gesso

Quadro de isolamento

Sistemas de isolamento PU

Sistemas de spray térmico e acústico

Tampas de tubos

Tubos pré-isolados

Âncoras químicas
Energia e Recursos
Indústria Eletrônica e Elétrica
Indústria alimentícia
Indústria de móveis
Isolamento por pulverização
Limpeza e Lavagem
Lubrificantes e fluidos para usinagem de metais
Papel de celulose
Exemplos de características do produto
Plásticos e Borrachas
Prevenção de incêndio
Revestimentos e tintas
Transporte
Têxteis e Couros
Produtos de consumo

Sabonetes líquidos

Tira-manchas de tecido

Produtos de limpeza e manutenção de móveis

Limpadores de cozinha

Limpadores de banheiro

Limpadores de janela

Fluidos sanitários

Líquidos e loções para lavar louça

Condicionadores de tecidos e concentrados

Líquidos de lavagem e géis

Produtos multifuncionais

Produtos para lava-louças
Surfactantes















































































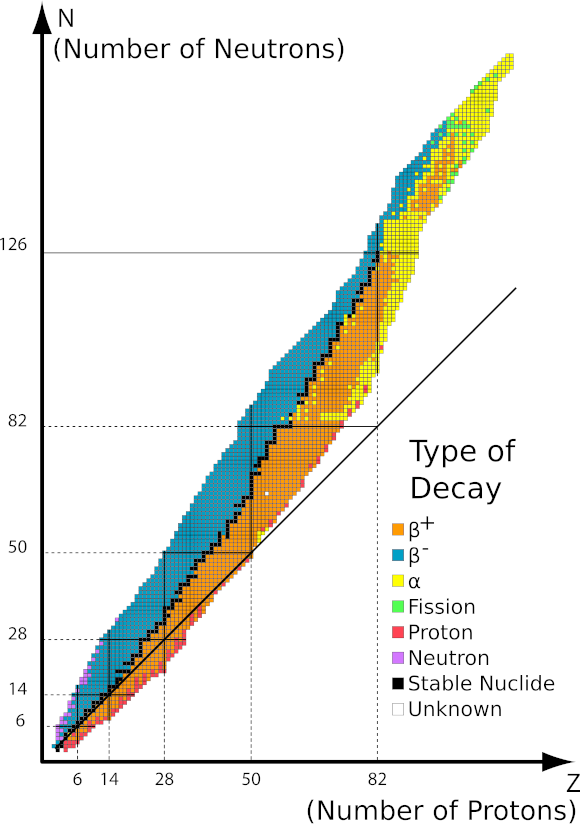
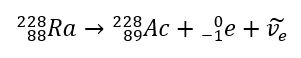 Esta radiação é caracterizada por partículas carregadas negativamente com um alcance de várias dezenas de centímetros no ar e maior permeabilidade em comparação com a radiação alfa. É retido por uma folha de alumínio com uma espessura de cerca de 3 a 4 mm. O decaimento beta-plus ocorre de forma semelhante, mas emite partículas de pósitrons e neutrinos de elétrons. O número de prótons no núcleo diminui e o elemento que o sofre é transformado em outro de número atômico menor, como no exemplo:
Esta radiação é caracterizada por partículas carregadas negativamente com um alcance de várias dezenas de centímetros no ar e maior permeabilidade em comparação com a radiação alfa. É retido por uma folha de alumínio com uma espessura de cerca de 3 a 4 mm. O decaimento beta-plus ocorre de forma semelhante, mas emite partículas de pósitrons e neutrinos de elétrons. O número de prótons no núcleo diminui e o elemento que o sofre é transformado em outro de número atômico menor, como no exemplo: