Fenomén radioaktivity (neboli radioaktivní emise) byl poprvé pozorován při experimentu Henriho Becquerela na rentgenovém záření (Rentgenové záření) v roce 1896. Jeho experiment měl potvrdit tezi o materiálech vyrobených z uranu, podle kterých měl emitovat X- paprsky po absorbování slunečního světla.

K provedení testu byl použit fotografický film, který vlivem těchto paprsků zčernal. Experiment ukázal, že sluneční záření není nutné, aby testovaný materiál film zčernal. To však bylo v rozporu s původní hypotézou, takže musel být proveden další výzkum. Tentokrát bylo úkolem potvrdit nebo vyvrátit rentgenové záření jako faktor způsobující změnu ve filmu. Bylo využito toho, že rentgenové záření nenese žádný náboj, takže se neohýbá magnetickým polem. Becquerel umístil materiál obsahující uran a fotografický film do vakuové komory umístěné v magnetickém poli. V důsledku experimentu bylo zjištěno, že paprsky vyzařované testovaným vzorkem se ohýbají v magnetickém poli, což znamená, že není totéž jako rentgenové záření. V průběhu svého výzkumu vědec ukázal, že existují tři typy záření, které mohou materiály vyzařovat – neutrální, kladně nabité a záporně nabité. Na základě těchto předpokladů následující výzkumníci předložili své teze a provedli další experimenty. Maria Skłodowska Curie a Pierre Curie objevili další radioaktivní prvky: polonium a radium. Ernest Rutherford, nositel Nobelovy ceny za chemii , také věnoval část své kariéry radioaktivitě a pojmenoval typy záření objevené Becquerelem řeckými písmeny abecedy: alfa, beta a gama.
Výzkum ukázal, že radioaktivita je rysem některých prvků. To ukazuje na jeho úzký vztah s jejich atomovou úrovní, a přesněji – s atomovým jádrem. Každý ze tří typů záření je kvantem energie, které může nestabilní jádro emitovat. To znamená, že záření je vlastně výsledkem jejich rozpadu. Výskyt těchto nestabilních jader je v praxi způsoben jejich poměrem protonů k neutronům. Vzhledem k různým typům nestability existují také různé druhy záření. Klíčem k pochopení radioaktivity jsou izotopy a jejich rozdíly na atomové úrovni. Například nejběžnější izotop uhlíku 12C není radioaktivní, zatímco 14C je radioaktivní. Jejich atomové číslo , a tedy i počet protonů, je stejné. Rozdíl také nemůže být způsoben počtem elektronů, protože atom by pak byl kladně nebo záporně nabitý iont. Jedinou možností jsou v případě izotopů rozdíly v počtu neutronů v jádře. 14 C má o dva neutrony více než 12 C, takže je také těžší. Existence izotopů pro všechny prvky znamená, že počet radioaktivních jader je také velký. Takové nestabilní a radioaktivní izotopy se nazývají radioizotopy, ale jejich prevalence není tak vysoká jako ty viditelné v periodické tabulce prvků .
Protony a neutrony v jádře jsou vystaveny velkým jaderným silám, které je drží pohromadě a překonávají elektrostatické odpuzování mezi protony. Na rozdíl od protonů mají neutrony pozitivní vliv na posílení jaderné síly. Ukázalo se, že poměr počtu neutronů a protonů by měl být asi 1,5:1. Pro lehčí atomy pod 20u je stabilní poměr 1:1. Jinak mají jádra tendenci se rozpadat. Všechny izotopy prvků s atomovou hmotností nad 208 jsou nestabilní.
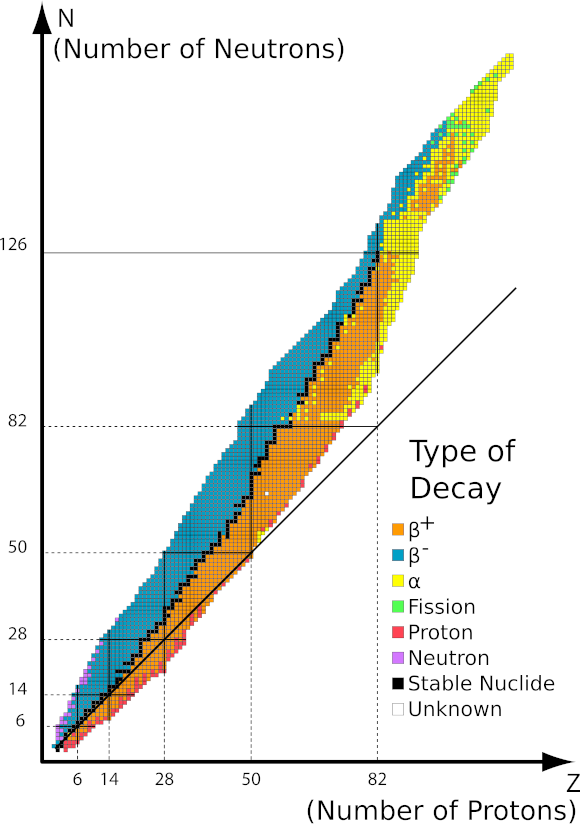
Obrázek 1 Graf oblasti stability v závislosti na počtu nukleonů v jádře. Zdroj: http://ch302.cm.utexas.edu/nuclear/radioactivity/selector.php?name=band-stability
Tyto typy rozpadů zahrnují změnu počtu protonů v jádře, a tedy i změnu chemického prvku z jednoho na druhý.
Experimentálně v roce 1909 E. Rutherford a T. Royds ukázali, že částice alfa jsou totožné s ionty helia. Po průchodu alfa záření tenkými stěnami vakuové komory to jasně potvrdil snímek spektrálních čar na optickém spektrometru získaný v plynové komoře. Například jádro 240 Pu prochází alfa zářením podle reakce: ![]() Alfa záření je charakterizováno kladně nabitými částicemi s dosahem několika centimetrů ve vzduchu a velmi nízkou propustností. Zastaví je kus papíru.
Alfa záření je charakterizováno kladně nabitými částicemi s dosahem několika centimetrů ve vzduchu a velmi nízkou propustností. Zastaví je kus papíru.
V případě záření beta-minus jsou emitovány elektrony přicházející z jádra. Jelikož se jádra nevyznačují přítomností elektronů, vznikají až při rozpadu a kromě nich je emitována i druhá částice – elektronové antineutrino. Vlivem nárůstu počtu protonů v molekule se beta rozpadový prvek přemění na jiný prvek s vyšším atomovým číslem. Příklad průběhu rozpadu je v souladu s tímto mechanismem: 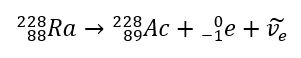 Toto záření je charakterizováno záporně nabitými částicemi s dosahem několika desítek centimetrů ve vzduchu a větší propustností ve srovnání s alfa zářením. Zastavuje ji hliníkový plech o tloušťce asi 3 až 4 mm. Beta-plus rozpad probíhá podobně, ale emituje pozitronové částice a elektronová neutrina. Počet protonů v jádře klesá a prvek, který to podstoupí, se přemění na jiný s nižším atomovým číslem, jako v příkladu:
Toto záření je charakterizováno záporně nabitými částicemi s dosahem několika desítek centimetrů ve vzduchu a větší propustností ve srovnání s alfa zářením. Zastavuje ji hliníkový plech o tloušťce asi 3 až 4 mm. Beta-plus rozpad probíhá podobně, ale emituje pozitronové částice a elektronová neutrina. Počet protonů v jádře klesá a prvek, který to podstoupí, se přemění na jiný s nižším atomovým číslem, jako v příkladu: 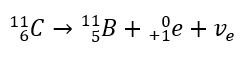
Je to jediný druh záření, který nemění prvek v jiný, protože nevyzařuje žádné částice, pouze samotné gama záření. Je to jeden z typů elektromagnetických vln, podobně jako infračervené nebo ultrafialové světlo, ale vlna záření gama je nejkratší. Proces rozpadu způsobuje přechod excitovaného jádra atomu do stavu nižší energie, čímž dochází k emisi fotonů s energetickým ekvivalentem jádra atomu v jednotlivých stavech. Diagram průběhu gama rozpadu lze zapsat jako: ![]() Charakteristickým znakem gama záření je jeho identifikace s elektromagnetickým vlněním o vysoké frekvenci a světlem podobném. Dosah ve vzduchu je teoreticky neomezený, zatímco propustnost je největší ze všech typů radioaktivity. Zastaví ho jen silná zeď nebo patnácticentimetrová vrstva olova.
Charakteristickým znakem gama záření je jeho identifikace s elektromagnetickým vlněním o vysoké frekvenci a světlem podobném. Dosah ve vzduchu je teoreticky neomezený, zatímco propustnost je největší ze všech typů radioaktivity. Zastaví ho jen silná zeď nebo patnácticentimetrová vrstva olova.
Najděte si své místo ve skupině PCC. Seznamte se s naší nabídkou a rozvíjejte se s námi.
Neplacené letní stáže pro studenty a absolventy všech kurzů.