Aminokyseliny jsou skupinou organických sloučenin, jejichž struktura se skládá z atomů uhlíku, dusíku, vodíku a kyslíku a také z variabilní skupiny postranních řetězců. Jsou to bifunkční sloučeniny, jejichž molekuly zahrnují karboxylové skupiny COOH a aminové skupiny NH2 .

Obecný vzorec aminokyselin je následující: NH 2 – R – COOH Jejich název je zkrácenou formou výrazu „α-aminokarboxylová kyselina“. Když mluvíme o různých typech aminokyselin, často nahrazujeme jejich systematické názvy obvyklými názvy. Abychom uvedli příklad, kyselina aminooctová se nazývá glycin, kyselina 2-aminopropanová se nazývá alanin a kyselina 2-amino-3-methylbutanová se nazývá valin.
Klasifikace aminokyselin
Hlavní rozdělení aminokyselin je na proteinové a nebílkovinné typy. První skupina zahrnuje kolem 20 sloučenin, z nichž každá je součástí bílkovin a je pro lidský organismus klíčová. Tyto proteiny, které také existují jako strukturální molekuly v rostlinách a zvířatech, hrají zásadní roli tím, že se účastní mnoha mechanismů odpovědných za udržování homeostázy v lidských tělech. Další klasifikace zohledňuje možnost produkovat konkrétní aminokyselinu nebo její požadovaný přísun do lidského těla spolu s potravou.
Exogenní a endogenní aminokyseliny
Exogenní aminokyseliny jsou organické sloučeniny potřebné k udržení homeostázy v našem těle, ale nejsou schopny vlastní produkce. Proto musí být dodávány ve formě vhodné stravy spolu se správně vyváženou stravou a ve formě adekvátních doplňků. Tato skupina aminokyselin zahrnuje:
- Lysin – antivirová aminokyselina, která zlepšuje imunitu;
- methionin, který řídí produkci růstového hormonu;
- Threonin, který je zodpovědný za správné udržování vlhkosti pokožky a správné fungování nervového systému;
- Leucin, jehož hlavní úlohou je kontrolovat hladinu vylučovaného kortizolu a cukru a také podporovat hojení ran;
- Isoleucin – aminokyselina, která se účastní procesů svalového metabolismu se zvláštním zaměřením na svalové tkáně;
- Valin, který podporuje regeneraci svalů a odstranění přebytečné tukové tkáně;
- Tryptofan, prekurzor serotoninu, který má zvýšit kvalitu spánku, zlepšit fyzický a duševní stav a kontrolovat chuť k jídlu;
- Fenylalanin, který je prekurzorem mnoha hormonů důležitých pro lidské tělo, včetně tyrosinu, dopaminu, epinefrinu a noradrenalinu.
Do druhé kategorie patří endogenní aminokyseliny , které jsou v lidském těle pravidelně syntetizovány, takže poptávka po nich je neustále autonomně pokryta. Tato skupina obsahuje více aminokyselin, které zahrnují:
- Alanin – aminokyselina zodpovědná za přenos glukózy do červených krvinek a mozku;
- Kyselina asparagová, která zlepšuje kognitivní funkce a schopnost koncentrace;
- Asparagin, který podporuje mnoho procesů, jako je učení, zapamatování nebo zlepšení koncentrace;
- Kyselina glutamová, která podporuje trávicí procesy, snižuje pocit únavy a podporuje paměť.
Podmíněné aminokyseliny
Jedná se o sloučeniny, které mohou být produkovány v těle, ale pouze v případě přístupu k odpovídajícímu množství jejich prekurzorů. Podmíněné aminokyseliny zahrnují:
- Arginin, který oddaluje stárnutí, zkracuje dobu hojení ran a zlepšuje fyzickou kondici;
- Cystein, který je stavebním materiálem při tvorbě glutathionu a je důležitým výrobním prvkem kolagenu;
- Glutamin, který podporuje činnost střev a odstraňování zbytečných metabolických produktů z lidského těla;
- Tyrosin, který se stejně jako cystein podílí na tvorbě kolagenu, ale je také nezbytný pro syntézu melaninu a pomáhá udržovat homeostázu štítné žlázy;
- Glycin, což je aminokyselina schopná léčit artritidu a diabetes;
- Ornitin, který je schopen snížit hladinu kortizolu, zlepšit kvalitu spánku a zvýšit účinnost střevních funkcí a trávicích enzymů;
- Prolin, který příznivě ovlivňuje stav pokožky a zlepšuje její pružnost;
- Serin, orientovaný na procesy, které podporují imunitní systém a fungování neuronů.
Proteinové aminokyseliny
Jak název napovídá, součástí bílkovin jsou také aminokyseliny. Přesněji řečeno, proteiny jsou různé typy aminokyselin, které jsou vzájemně kombinovány. Je jich dvacet a při syntéze jsou kódovány tzv. kodony (sekvence tří nukleotidů obsažených v mRNa, které tvoří kódující jednotku). Každá z nich má dva společné rysy: jsou to alfa- a L-aminokyseliny. To znamená, že jejich aminová skupina je napojena na alfa-uhlík, který přímo sousedí s karbonylovou skupinou. Písmeno „L“ znamená stereoizomer ve Fischerově projekci, takže aminová skupina je umístěna na levé straně vzorce. 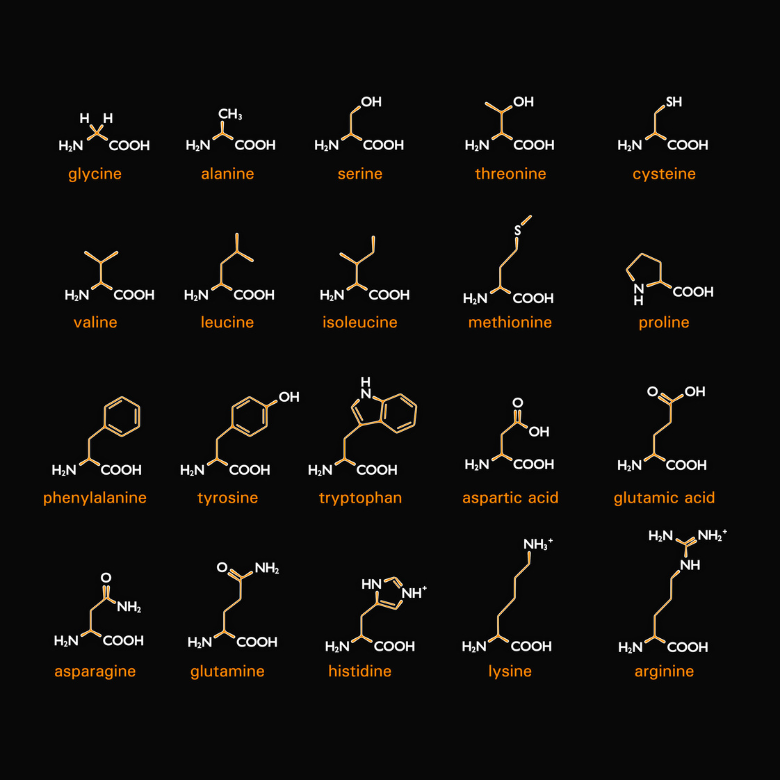
Fyzikálně-chemické vlastnosti aminokyselin
Fyzikální forma aminokyselin je obvykle krystalická pevná látka se sladkou chutí. Jejich rozpustnost ve vodě je dobrá, ale nerozpouštějí se v organických rozpouštědlech. Jejich teploty tání jsou poměrně vysoké. Chemická povaha aminokyselin je amfoterní a reakce jejich vodných roztoků je neutrální. Disociace produkuje duální ionty, které jsou výsledkem neutralizace základní aminové skupiny karboxylovým radikálem. To vede k produkci vnitřní amonné soli, která vykazuje oba náboje: kladný i záporný. Jejich množství je stejné. Aminokyselina může existovat jako kation nebo anion v závislosti na prostředí, ve kterém se disociuje. U kyselých reakcí karboxylová skupina nedisociuje a aminokyselina má kladný náboj. V alkalickém prostředí se reakce posouvají směrem k produkci záporného iontu.
izoelektrický bod (pI)
Je to bod, kde má aminokyselina formu duálního iontu. Pro každou molekulu můžeme upravit adekvátní koncentraci iontů [H 3 O +], tedy takové pH, kdy se ionty nepohybují v elektrickém poli. Amfoterní povaha aminokyselin a jejich existence ve formě duálních iontů implikuje iontovou strukturu solí při působení kyselin a zásad. Experimentální stanovení izoelektrického bodu se provádí přidáním aminokyseliny, například kaseinu, do vhodných zkumavek obsahujících roztoky (CH 3 COOH a CH 3 COONa) se známými koncentracemi pH. Izoelektrického bodu je dosaženo tam, kde je ložisko nejhojnější. Vzhledem k charakteristice izoelektrického bodu jej můžeme použít k separaci směsi proteinů pomocí elektroforézy. Tato metoda je založena na kyselo-bazických vlastnostech aminokyselin a směs se umístí na navlhčený papír. S použitím známého pH můžeme určit formu, ve které budou jednotlivé aminokyseliny existovat. Pak, pokud přivedeme napětí na papír, budou se kladně nabité aminokyseliny pohybovat směrem ke katodě (-) a ty se záporným nábojem k anodě (+). Neutrálně nabité sloučeniny, vyvážené kladnými a zápornými náboji v molekule, zůstanou na stejném místě.
Reakce charakteristické pro karboxylovou skupinu
- Esterifikace, která spočívá v syntéze esterů produkovaných reakcí mezi aminokyselinou a alkoholem. Produkt takové reakce nevykazuje amfoterní povahu, ale vykazuje vlastnosti použitého aminu.
- Dekarboxylace, což je zahřívání aminokyseliny v přítomnosti roztoku hydroxidu barnatého (Ba(OH) 2 ). Transformací vznikají aminy.
- Tvorba komplexů souvisí se schopností aminokyselin vázat se s kationty kovu, zejména mědi, což způsobuje tvorbu barevných sloučenin (komplexních solí).

Reakce charakteristické pro aminovou skupinu
- Deaminace, která se týká aminokyselin, které obsahují primární aminovou skupinu. Reakce probíhá pod vlivem kyseliny dusičné (HNO 2 ) a aminokyselina použitá jako reaktant oxiduje a vytváří hydracidu. Aminová skupina se uvolňuje ve formě dusíku. Existuje několik typů deaminace, včetně hydrolytické deaminace, hydrolytické deaminace s dekarboxylací, deaminace redukcí a desaturační deaminace.
- Oxidace, která způsobuje přeměnu aminokyselin na ketokyseliny.
- Biochemické reakce – všechny aminokyseliny, které lze klasifikovat jako Schiffovy báze, jsou schopné biochemických přeměn, jako je transmitance a dekarboxylace.
Reakce používané pro detekci aminokyselin
- Ninhydrinová reakce je barevná reakce, kde reaktanty jsou aminokyselina a činidlo ve formě roztoku ninhydrinu. Reakcí vzniká charakteristická fialovomodrá barva.
- Xantoproteinová reakce je příkladem cesty k detekci aromatických aminokyselin, jako je fenylalanin, tyrosin nebo tryptofan. Sloučenina vystavená působení koncentrovaného roztoku kyseliny dusičné ( HN03 ) změní svou barvu na žlutou. Je výsledkem produkce derivátů dusičné aminokyseliny během reakce.
Zdroje aminokyselin
Abychom zajistili dobrou fyzickou i psychickou kondici lidského těla, měli bychom mu zajistit přiměřené množství každého stavebního materiálu včetně aminokyselin. Mimořádně důležitým zdrojem všech aminokyselin potřebných pro správné fungování jsou kompletní bílkoviny. Patří mezi ně maso, zejména drůbež, ryby, vejce a mléčné výrobky. Mléko obsahuje vysoké množství leucinu, isoleucinu, threoninu a tryptofanu. Lysin a methionin lze nalézt v sóji. Valin lze dodávat společně s rýží, arašídy, sezamem a mandlemi, zatímco fenylalanin začleněním vajec, sýrů a obilných výrobků do naší stravy. Přítomnost aminokyselin v potravinách je běžná, ale aby byla naše strava správně vyvážená, měly by být produkty, které používáme, diverzifikované. Obsahují totiž jen určité aminokyseliny ze skupiny nezbytné pro udržení správných životních funkcí.





























































































































