Les acides aminés sont un groupe de composés organiques dont la structure est constituée d'atomes de carbone, d'azote, d'hydrogène et d'oxygène ainsi que d'un groupe de chaîne latérale variable. Ce sont des composés bifonctionnels dont les molécules comprennent des groupes carboxyle COOH et des groupes amine NH 2 .

La formule générale des acides aminés est la suivante : NH 2 – R – COOH Leur nom est une forme abrégée du terme « acide α-amino carboxylique ». Lorsque nous parlons de différents types d’acides aminés, nous remplaçons souvent leurs noms systématiques par des noms usuels. Pour donner un exemple, l’acide aminoacétique est appelé glycine, l’acide 2-aminopropanoïque est appelé alanine et l’acide 2-amino-3-méthylbutanoïque est appelé valine.
Classification des acides aminés
La principale division des acides aminés est en types protéiques et non protéiques. Le premier groupe comprend environ 20 composés, dont chacun est un composant des protéines et est crucial pour le corps humain. Ces protéines, qui existent également sous forme de molécules structurales chez les plantes et les animaux, jouent un rôle fondamental en participant à de nombreux mécanismes responsables du maintien de l’homéostasie du corps humain. Une autre classification prend en compte la possibilité de produire un acide aminé particulier ou son apport nécessaire au corps humain en même temps que la nourriture.
Acides aminés exogènes et endogènes
Les acides aminés exogènes sont des composés organiques nécessaires au maintien de l’homéostasie de notre corps, mais ils ne sont pas capables de s’auto-produire. C’est pourquoi ils doivent être apportés sous forme d’une alimentation adaptée accompagnée de repas bien équilibrés et sous forme de compléments adéquats. Ce groupe d’acides aminés comprend :
- Lysine – un acide aminé antivirus qui améliore l’immunité ;
- La méthionine, qui contrôle la production de l’hormone de croissance ;
- La thréonine, qui est responsable du bon maintien de l’hydratation de la peau et du bon fonctionnement du système nerveux ;
- La leucine, dont le rôle principal est de contrôler les niveaux de cortisol et de sucre sécrétés ainsi que de favoriser la cicatrisation des plaies ;
- Isoleucine – un acide aminé qui participe aux processus du métabolisme musculaire, avec un accent particulier sur les tissus musculaires ;
- Valine, qui favorise la récupération musculaire et l’élimination des excès de tissu adipeux ;
- Le tryptophane, précurseur de la sérotonine, qui doit augmenter la qualité du sommeil, améliorer l’état physique et mental et contrôler l’appétit ;
- La phénylalanine est un précurseur de nombreuses hormones importantes pour le corps humain, notamment la tyrosine, la dopamine, l’épinéphrine et la noradrénaline.
L’autre catégorie comprend les acides aminés endogènes , qui sont régulièrement synthétisés dans le corps humain, de sorte que leur demande est constamment couverte de manière autonome. Ce groupe contient plus d’acides aminés, notamment :
- Alanine – un acide aminé responsable du transport du glucose vers les globules rouges et le cerveau ;
- L’acide aspartique, qui améliore les fonctions cognitives et la capacité de concentration ;
- L’asparagine, qui soutient de nombreux processus tels que l’apprentissage, la mémorisation ou l’amélioration de la concentration ;
- L’acide glutamique, qui soutient les processus de digestion, réduit la sensation de fatigue et soutient la mémoire.
Acides aminés conditionnels
Ce sont des composés qui peuvent être produits dans l’organisme, mais uniquement en cas d’accès à des quantités appropriées de leurs précurseurs. Les acides aminés conditionnels comprennent :
- L’arginine, qui retarde le vieillissement, réduit le temps de cicatrisation des plaies et améliore la forme physique ;
- La cystéine, qui est un matériau de construction dans la formation du glutathion et un élément important de la production de collagène ;
- Glutamine, qui soutient le fonctionnement des intestins et l’élimination des produits métaboliques inutiles du corps humain ;
- La Tyrosine, qui, tout comme la cystéine, participe à la production de collagène, mais est également nécessaire à la synthèse de mélanine et participe au maintien de l’homéostasie de la glande thyroïde ;
- La glycine, qui est un acide aminé capable de guérir l’arthrite et le diabète ;
- L’ornithine, qui est capable de réduire le niveau de cortisol, d’améliorer la qualité du sommeil et d’améliorer l’efficacité des fonctions intestinales et des enzymes digestives ;
- La Proline, qui affecte favorablement l’état de la peau et améliore sa souplesse ;
- Sérine, orientée vers les processus qui soutiennent le système immunitaire et le fonctionnement des neurones.
Acides aminés protéiques
Comme son nom l’indique, certains acides aminés sont également des composants des protéines. Plus précisément, les protéines sont différents types d’acides aminés combinés les uns aux autres. Il y en a vingt et lors de la synthèse, ils sont codés par ce qu’on appelle des codons (séquences de trois nucléotides contenues dans l’ARNm, qui constituent l’unité codante). Chacun d’eux a deux caractéristiques communes : ce sont les acides alpha- et L-aminés. Cela signifie que leur groupe amine est connecté au carbone alpha, qui est directement adjacent au groupe carbonyle. La lettre « L » représente un stéréoisomère dans la projection de Fischer, le groupe amine est donc situé sur le côté gauche de la formule. 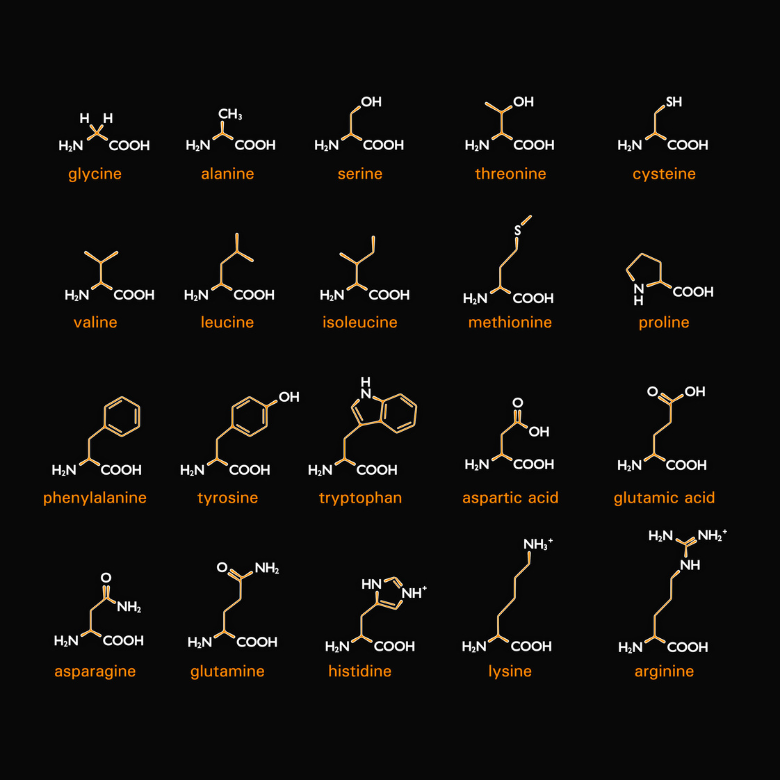
Les propriétés physico-chimiques des acides aminés
La forme physique des acides aminés est généralement un solide cristallin au goût sucré. Leur solubilité dans l’eau est bonne, mais ils ne se dissolvent pas dans les solvants organiques. Leurs points de fusion sont relativement élevés. La nature chimique des acides aminés est amphotère et la réaction de leurs solutions aqueuses est neutre. La dissociation produit des ions doubles, qui résultent de la neutralisation du groupe amine basique par un radical carboxyle. Cela aboutit à la production d’un sel d’ammonium interne qui présente les deux charges : positive et négative. Leurs quantités sont égales. Un acide aminé peut exister sous forme de cation ou d’anion, selon l’environnement dans lequel il se dissocie. Pour les réactions acides, le groupe carboxyle ne se dissocie pas et l’acide aminé a une charge positive. Dans un environnement alcalin, les réactions évoluent vers la production d’un ion négatif.
Le point isoélectrique (pI)
C’est un point où un acide aminé prend la forme d’un double ion. Pour chaque molécule, nous pouvons ajuster une concentration adéquate d’ions [H 3 O +], c’est-à-dire un pH où les ions ne se déplacent pas dans le champ électrique. La nature amphotère des acides aminés et leur existence sous forme d’ions doubles impliquent une structure ionique des sels lorsqu’ils sont affectés par les acides et les alcalis. La détermination expérimentale du point isoélectrique est réalisée en ajoutant un acide aminé, par exemple de la caséine, dans des tubes à essai appropriés contenant des solutions (CH 3 COOH et CH 3 COONa) de concentrations de pH connues. Le point isoélectrique est atteint là où le dépôt est le plus abondant. Compte tenu de la caractéristique du point isoélectrique, nous pouvons l’utiliser pour séparer un mélange de protéines grâce à l’électrophorèse. Cette méthode est basée sur les propriétés acido-basiques des acides aminés et le mélange est placé sur du papier mouillé. En utilisant un pH connu, nous pouvons déterminer la forme sous laquelle des acides aminés particuliers existeront. Ensuite, si nous alimentons le papier en tension, les acides aminés chargés positivement se déplaceront vers la cathode (-), et ceux qui ont une charge négative, vers l’anode (+). Les composés chargés neutrement, équilibrés par les charges positives et négatives de la molécule, resteront au même endroit.
Réactions caractéristiques du groupe carboxyle
- L’estérification, qui consiste à synthétiser des esters produits par une réaction entre un acide aminé et un alcool. Le produit d’une telle réaction ne présente pas de caractère amphotère, mais présente les propriétés de l’aminé utilisée.
- La décarboxylation, c’est-à-dire le chauffage d’un acide aminé en présence d’une solution d’hydroxyde de baryum (II) (Ba(OH) 2 ). La transformation produit des amines.
- La production de complexes est liée à la capacité des acides aminés à se lier aux cations d’un métal, principalement le cuivre, ce qui provoque la formation de composés colorés (sels complexes).

Réactions caractéristiques du groupe amine
- La désamination, qui concerne les acides aminés contenant le groupe amine primaire. La réaction se produit sous l’influence de l’acide nitrique (III) (HNO 2 ), et l’acide aminé utilisé comme réactif s’oxyde et produit un hydracide. Le groupe amine est libéré sous forme d’azote. Il existe plusieurs types de désamination, notamment la désamination hydrolytique, la désamination hydrolytique avec décarboxylation, la désamination par réduction et la désamination par désaturation.
- L’oxydation, qui provoque la conversion des acides aminés en acides céto.
- Réactions biochimiques – tous les acides aminés pouvant être classés comme bases de Schiff sont capables de transformations biochimiques telles que la transmission et la décarboxylation.
Réactions utilisées pour détecter les acides aminés
- La réaction à la ninhydrine est une réaction colorée où les réactifs sont un acide aminé et un réactif sous forme de solution de ninhydrine. La réaction produit une couleur bleu-violet caractéristique.
- La réaction des xanthoprotéines est un exemple de méthode permettant de détecter des acides aminés aromatiques, tels que la phénylalanine, la tyrosine ou le tryptophane. Un composé soumis à une solution concentrée d’acide nitrique (V) (HNO 3 ) change de couleur en jaune. C’est le résultat de la production de dérivés d’acides aminés nitriques au cours de la réaction.
Sources d’acides aminés
Pour assurer une bonne condition physique et mentale du corps humain, nous devons lui fournir des quantités appropriées de chaque matériau de construction, y compris les acides aminés. Les protéines complètes constituent une source extrêmement importante de tous les acides aminés nécessaires au bon fonctionnement. Ils comprennent la viande, en particulier la volaille, le poisson, les œufs et les produits laitiers. Le lait contient de grandes quantités de leucine, d’isoleucine, de thréonine et de tryptophane. La lysine et la méthionine peuvent être trouvées dans le soja. La valine peut être apportée avec le riz, les cacahuètes, le sésame et les amandes, ainsi que la phénylalanine, en incluant des œufs, des fromages et des produits céréaliers dans notre alimentation. La présence d’acides aminés dans les produits alimentaires est courante, mais pour que notre alimentation soit bien équilibrée, les produits que nous utilisons doivent être diversifiés. En effet, ils ne contiennent que certains acides aminés du groupe nécessaire au maintien de fonctions vitales appropriées.





























































































































