Los aminoácidos son un grupo de compuestos orgánicos cuya estructura consta de átomos de carbono, nitrógeno, hidrógeno y oxígeno, así como de un grupo de cadena lateral variable. Son compuestos bifuncionales cuyas moléculas incluyen grupos carboxilo COOH y grupos amina NH2 .

La fórmula general de los aminoácidos es la siguiente: NH 2 – R – COOH Su nombre es una forma abreviada del término “ácido α-aminocarboxílico”. Cuando hablamos de diferentes tipos de aminoácidos, a menudo sustituimos sus nombres sistemáticos por nombres habituales. Por poner un ejemplo, el ácido aminoacético se llama glicina, el ácido 2-aminopropanoico se llama alanina y el ácido 2-amino-3-metilbutanoico se llama valina.
Clasificación de aminoácidos.
La principal división de los aminoácidos es en tipos proteicos y no proteicos. El primer grupo incluye alrededor de 20 compuestos, cada uno de los cuales es un componente de las proteínas y es crucial para el cuerpo humano. Estas proteínas, que también existen como moléculas estructurales en plantas y animales, juegan un papel fundamental al participar en muchos mecanismos responsables del mantenimiento de la homeostasis en el cuerpo humano. Otra clasificación tiene en cuenta la posibilidad de producir un determinado aminoácido o su suministro necesario al cuerpo humano junto con los alimentos.
Aminoácidos exógenos y endógenos.
Los aminoácidos exógenos son compuestos orgánicos necesarios para mantener la homeostasis en nuestro cuerpo, pero no son capaces de autoproducirse. Por este motivo, deben suministrarse en forma de una dieta adecuada, acompañada de comidas adecuadamente equilibradas y en forma de suplementos adecuados. Este grupo de aminoácidos incluye:
- Lisina – un aminoácido antivirus que mejora la inmunidad;
- Metionina, que controla la producción de la hormona del crecimiento;
- Treonina, que se encarga del correcto mantenimiento de la humedad de la piel y del buen funcionamiento del sistema nervioso;
- Leucina, cuya función principal es controlar el nivel de cortisol secretado y los niveles de azúcar, así como favorecer la cicatrización de heridas;
- Isoleucina: un aminoácido que participa en los procesos del metabolismo muscular, con especial atención en los tejidos musculares;
- Valina, que favorece la recuperación muscular y la eliminación del exceso de tejido graso;
- Triptófano, precursor de la serotonina, que aumenta la calidad del sueño, mejora el estado físico y mental y controla el apetito;
- La fenilalanina es un precursor de muchas hormonas importantes para el cuerpo humano, incluidas la tirosina, la dopamina, la epinefrina y la noradrenalina.
La otra categoría incluye los aminoácidos endógenos , que se sintetizan regularmente en el cuerpo humano, por lo que su demanda se cubre constantemente de forma autónoma. Este grupo contiene más aminoácidos, que incluyen:
- Alanina: un aminoácido responsable de transportar glucosa a los glóbulos rojos y al cerebro;
- Ácido aspártico, que mejora las funciones cognitivas y la capacidad de concentración;
- Asparagina, que apoya muchos procesos como el aprendizaje, la memorización o la mejora de la concentración;
- El ácido glutámico, que favorece los procesos de digestión, reduce la sensación de fatiga y favorece la memoria.
aminoácidos condicionales
Se trata de compuestos que el organismo puede producir, pero sólo si se accede a cantidades adecuadas de sus precursores. Los aminoácidos condicionales incluyen:
- Arginina, que retrasa el envejecimiento, reduce el tiempo de cicatrización de las heridas y mejora la condición física;
- cisteína, que es un material de construcción en la formación de glutatión y es un importante elemento de producción de colágeno;
- Glutamina, que favorece el funcionamiento de los intestinos y la eliminación de productos metabólicos innecesarios del cuerpo humano;
- tirosina, que, al igual que la cisteína, participa en la producción de colágeno, pero también es necesaria para la síntesis de melanina y ayuda a mantener la homeostasis de la glándula tiroides;
- Glicina, que es un aminoácido capaz de curar la artritis y la diabetes;
- Ornitina, que es capaz de reducir el nivel de cortisol, mejorar la calidad del sueño y mejorar la eficiencia de las funciones intestinales y las enzimas digestivas;
- Prolina, que afecta favorablemente el estado de la piel y mejora su flexibilidad;
- Serina, orientada a procesos que apoyan el sistema inmunológico y el funcionamiento de las neuronas.
Aminoácidos proteicos
Como sugiere el nombre, también hay aminoácidos que son componentes de las proteínas. Más concretamente, las proteínas son varios tipos de aminoácidos combinados entre sí. Hay veinte y durante la síntesis se codifican mediante los llamados codones (secuencias de tres nucleótidos contenidos en el ARNm, que constituyen la unidad de codificación). Cada uno de ellos tiene dos características comunes: son alfa y L-aminoácidos. Esto significa que su grupo amino está unido al carbono alfa, que está directamente al lado del grupo carbonilo. La letra "L" representa un estereoisómero en la proyección de Fischer, por lo que el grupo amina se encuentra en el lado izquierdo de la fórmula. 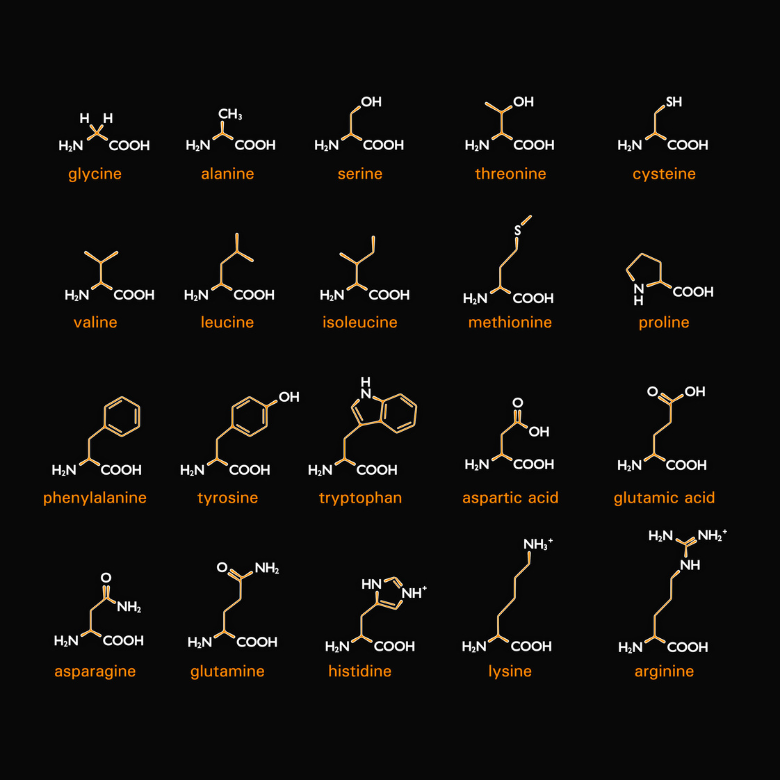
Las propiedades físico-químicas de los aminoácidos.
La forma física de los aminoácidos suele ser un sólido cristalino que tiene un sabor dulce. Su solubilidad en agua es buena, pero no se disuelven en disolventes orgánicos. Sus puntos de fusión son relativamente altos. La naturaleza química de los aminoácidos es anfótera y la reacción de sus soluciones acuosas es neutra. La disociación produce iones duales, que son el resultado de neutralizar el grupo amino básico con un radical carboxilo. Esto da como resultado la producción de una sal de amonio interna que muestra ambas cargas: positiva y negativa. Sus cantidades son iguales. Un aminoácido puede existir como catión o anión, dependiendo del entorno en el que se disocia. Para reacciones ácidas, el grupo carboxilo no se disocia y el aminoácido tiene carga positiva. En un ambiente alcalino, las reacciones se desplazan hacia la producción de un ion negativo.
El punto isoeléctrico (pI)
Es un punto donde un aminoácido toma la forma de un ion dual. Para cada molécula, podemos ajustar una concentración adecuada de iones [H 3 O +], es decir, un pH en el que los iones no se mueven en el campo eléctrico. La naturaleza anfótera de los aminoácidos y su existencia en forma de iones duales implica una estructura iónica de sales cuando se ven afectadas por ácidos y álcalis. La determinación experimental del punto isoeléctrico se lleva a cabo añadiendo un aminoácido, por ejemplo caseína, en tubos de ensayo apropiados que contienen soluciones (CH 3 COOH y CH 3 COONa) con concentraciones de pH conocidas. El punto isoeléctrico se alcanza donde el depósito es más abundante. Dada la característica del punto isoeléctrico, podemos utilizarlo para separar una mezcla de proteínas mediante electroforesis. Este método se basa en las propiedades ácido-básicas de los aminoácidos y la mezcla se coloca sobre papel humedecido. Con el uso de un pH conocido, podemos determinar la forma en que existirán aminoácidos particulares. Luego, si suministramos tensión al papel, los aminoácidos cargados positivamente se desplazarán hacia el cátodo (-), y los de carga negativa, hacia el ánodo (+). Los compuestos con carga neutra, equilibrados por las cargas positivas y negativas de la molécula, permanecerán en el mismo lugar.
Reacciones características del grupo carboxilo.
- Esterificación, que consiste en sintetizar ésteres producidos por una reacción entre un aminoácido y un alcohol. El producto de tal reacción no presenta naturaleza anfótera, pero sí las propiedades de la amina utilizada.
- Descarboxilación, es decir, el calentamiento de un aminoácido en presencia de una solución de hidróxido de bario (II) (Ba(OH) 2 ). La transformación produce aminas.
- La producción de complejos está relacionada con la capacidad de los aminoácidos de unirse con los cationes de un metal, principalmente cobre, lo que provoca la formación de compuestos coloreados (sales complejas).

Reacciones características del grupo amino.
- Deaminación, que se refiere a aminoácidos que contienen el grupo amino primario. La reacción se produce bajo la influencia del ácido nítrico (III) (HNO 2 ) y el aminoácido utilizado como reactivo se oxida y produce un hidrácido. El grupo amino se libera en forma de nitrógeno. Existen varios tipos de desaminación, incluida la desaminación hidrolítica, la desaminación hidrolítica con descarboxilación, la desaminación por reducción y la desaminación por desaturación.
- Oxidación, que hace que los aminoácidos se conviertan en cetoácidos.
- Reacciones bioquímicas: todos los aminoácidos que pueden clasificarse como bases de Schiff son capaces de realizar transformaciones bioquímicas como la transmitancia y la descarboxilación.
Reacciones utilizadas para detectar aminoácidos.
- La reacción de ninhidrina es una reacción coloreada donde los reactivos son un aminoácido y un reactivo en forma de solución de ninhidrina. La reacción produce un color azul violeta característico.
- La reacción de xantoproteínas es un ejemplo de vía para detectar aminoácidos aromáticos, como la fenilalanina, la tirosina o el triptófano. Un compuesto sometido a una solución concentrada de ácido nítrico (V) (HNO 3 ) cambia de color a amarillo. Es el resultado de la producción de derivados de aminoácidos nítricos durante la reacción.
Fuentes de aminoácidos
Para garantizar un buen estado físico y mental del cuerpo humano, debemos proporcionarle cantidades adecuadas de cada material de construcción, incluidos los aminoácidos. Una fuente extremadamente importante de todos los aminoácidos necesarios para el correcto funcionamiento son las proteínas completas. Incluyen carne, en particular aves, pescado, huevos y lácteos. La leche contiene altas cantidades de leucina, isoleucina, treonina y triptófano. La lisina y la metionina se encuentran en la soja. La valina se puede aportar junto con arroz, cacahuetes, sésamo y almendras, mientras que la fenilalanina, incluyendo huevos, quesos y productos cereales en nuestra dieta. La presencia de aminoácidos en los productos alimenticios es común, pero para que nuestra dieta esté correctamente equilibrada es necesario diversificar los productos que utilizamos. Esto se debe a que contienen sólo ciertos aminoácidos del grupo necesario para mantener las funciones vitales adecuadas.





























































































































