Aminokyseliny sú skupinou organických zlúčenín, ktorých štruktúra pozostáva z atómov uhlíka, dusíka, vodíka a kyslíka, ako aj skupiny s variabilným bočným reťazcom. Sú to bifunkčné zlúčeniny, ktorých molekuly zahŕňajú karboxylové skupiny COOH a amínové skupiny NH2 .

Všeobecný vzorec aminokyselín je nasledovný: NH 2 – R – COOH Ich názov je skrátenou formou výrazu „kyselina α-aminokarboxylová“. Keď hovoríme o rôznych typoch aminokyselín, často nahrádzame ich systematické názvy zaužívanými názvami. Aby sme uviedli príklad, kyselina aminooctová sa nazýva glycín, kyselina 2-aminopropánová sa nazýva alanín a kyselina 2-amino-3-metylbutánová sa nazýva valín.
Klasifikácia aminokyselín
Hlavné rozdelenie aminokyselín je na proteínové a nebielkovinové typy. Prvá skupina zahŕňa okolo 20 zlúčenín, z ktorých každá je súčasťou bielkovín a je pre ľudský organizmus kľúčová. Tieto proteíny, ktoré tiež existujú ako štrukturálne molekuly v rastlinách a zvieratách, hrajú základnú úlohu tým, že sa zúčastňujú mnohých mechanizmov zodpovedných za udržiavanie homeostázy v ľudskom tele. Iná klasifikácia zohľadňuje možnosť produkovať konkrétnu aminokyselinu alebo jej požadovaný prísun do ľudského tela spolu s potravou.
Exogénne a endogénne aminokyseliny
Exogénne aminokyseliny sú organické zlúčeniny potrebné na udržanie homeostázy v našom tele, no nie sú schopné vlastnej produkcie. Preto musia byť dodávané vo forme vhodnej stravy spolu s vhodne vyváženými jedlami a vo forme primeraných doplnkov. Táto skupina aminokyselín zahŕňa:
- Lyzín – antivírusová aminokyselina, ktorá zlepšuje imunitu;
- metionín, ktorý riadi produkciu rastového hormónu;
- Treonín, ktorý je zodpovedný za správne udržiavanie vlhkosti pokožky a správne fungovanie nervového systému;
- Leucín, ktorého hlavnou úlohou je kontrolovať hladinu vylučovaného kortizolu a cukru, ako aj podporovať hojenie rán;
- izoleucín – aminokyselina, ktorá sa podieľa na procesoch metabolizmu svalov s osobitným zameraním na svalové tkanivá;
- Valín, ktorý podporuje regeneráciu svalov a odstránenie prebytočného tukového tkaniva;
- Tryptofán, prekurzor serotonínu, ktorý má zvýšiť kvalitu spánku, zlepšiť fyzický a duševný stav a kontrolovať chuť do jedla;
- Fenylalanín, ktorý je prekurzorom mnohých hormónov dôležitých pre ľudské telo, vrátane tyrozínu, dopamínu, epinefrínu a noradrenalínu.
Do druhej kategórie patria endogénne aminokyseliny , ktoré sú v ľudskom tele pravidelne syntetizované, takže dopyt po nich je neustále autonómne pokrytý. Táto skupina obsahuje viac aminokyselín, medzi ktoré patria:
- Alanín – aminokyselina zodpovedná za prenos glukózy do červených krviniek a mozgu;
- Kyselina asparágová, ktorá zlepšuje kognitívne funkcie a schopnosť koncentrácie;
- Asparagín, ktorý podporuje mnohé procesy, ako je učenie, zapamätanie alebo zlepšenie koncentrácie;
- Kyselina glutámová, ktorá podporuje tráviace procesy, znižuje pocit únavy a podporuje pamäť.
Podmienené aminokyseliny
Sú to zlúčeniny, ktoré sa môžu v tele produkovať, ale len v prípade prístupu k primeraným množstvám ich prekurzorov. Podmienené aminokyseliny zahŕňajú:
- Arginín, ktorý odďaľuje starnutie, skracuje čas hojenia rán a zlepšuje fyzickú kondíciu;
- Cysteín, ktorý je stavebným materiálom pri tvorbe glutatiónu a je dôležitým výrobným prvkom kolagénu;
- Glutamín, ktorý podporuje činnosť čriev a odstraňovanie nepotrebných metabolických produktov z ľudského tela;
- tyrozín, ktorý sa rovnako ako cysteín podieľa na tvorbe kolagénu, ale je nevyhnutný aj pre syntézu melanínu a pomáha udržiavať homeostázu štítnej žľazy;
- Glycín, čo je aminokyselina schopná liečiť artritídu a cukrovku;
- Ornitín, ktorý je schopný znížiť hladinu kortizolu, zlepšiť kvalitu spánku a zvýšiť efektivitu črevných funkcií a tráviacich enzýmov;
- Prolín, ktorý priaznivo ovplyvňuje stav pokožky a zlepšuje jej pružnosť;
- Serine, orientovaný na procesy, ktoré podporujú imunitný systém a fungovanie neurónov.
Proteínové aminokyseliny
Ako už názov napovedá, súčasťou bielkovín sú aj aminokyseliny. Presnejšie povedané, proteíny sú rôzne typy aminokyselín, ktoré sa navzájom kombinujú. Je ich dvadsať a pri syntéze sú kódované takzvanými kodónmi (sekvencie troch nukleotidov obsiahnutých v mRNa, ktoré tvoria kódovaciu jednotku). Každá z nich má dva spoločné znaky: sú to alfa- a L-aminokyseliny. To znamená, že ich amínová skupina je napojená na alfa-uhlík, ktorý priamo susedí s karbonylovou skupinou. Písmeno „L“ znamená stereoizomér vo Fischerovej projekcii, takže amínová skupina sa nachádza na ľavej strane vzorca. 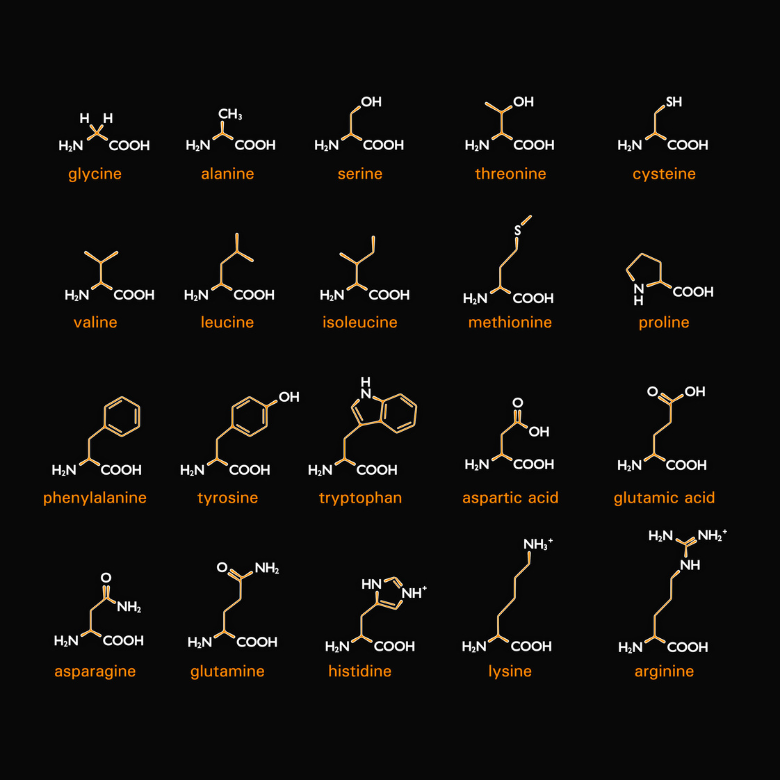
Fyzikálno-chemické vlastnosti aminokyselín
Fyzická forma aminokyselín je zvyčajne kryštalická pevná látka sladkej chuti. Ich rozpustnosť vo vode je dobrá, ale nerozpúšťajú sa v organických rozpúšťadlách. Ich teplota topenia je pomerne vysoká. Chemická povaha aminokyselín je amfotérna a reakcia ich vodných roztokov je neutrálna. Disociácia vytvára duálne ióny, ktoré sú výsledkom neutralizácie základnej amínovej skupiny karboxylovým radikálom. Výsledkom je vytvorenie vnútornej amónnej soli, ktorá vykazuje oba náboje: kladný aj záporný. Ich množstvá sú rovnaké. Aminokyselina môže existovať ako katión alebo anión v závislosti od prostredia, v ktorom sa disociuje. Pri kyslých reakciách sa karboxylová skupina nedisociuje a aminokyselina má kladný náboj. V alkalickom prostredí sa reakcie posúvajú smerom k produkcii záporného iónu.
Izoelektrický bod (pI)
Je to bod, kde aminokyselina nadobúda formu duálneho iónu. Pre každú molekulu vieme upraviť adekvátnu koncentráciu iónov [H 3 O +], teda také pH, kedy sa ióny nepohybujú v elektrickom poli. Amfotérna povaha aminokyselín a ich existencia vo forme duálnych iónov implikuje iónovú štruktúru solí, keď sú ovplyvnené kyselinami a zásadami. Experimentálne stanovenie izoelektrického bodu sa uskutočňuje pridaním aminokyseliny, napríklad kazeínu, do vhodných skúmaviek obsahujúcich roztoky ( CH3COOH a CH3COONa ) so známymi koncentráciami pH. Izoelektrický bod sa dosiahne tam, kde je ložisko najhojnejšie. Vzhľadom na charakteristiku izoelektrického bodu ho môžeme použiť na separáciu zmesi proteínov pomocou elektroforézy. Táto metóda je založená na kyslo-bázických vlastnostiach aminokyselín a zmes sa umiestni na navlhčený papier. Pomocou známeho pH môžeme určiť formu, v ktorej budú konkrétne aminokyseliny existovať. Potom, ak privedieme napätie na papier, kladne nabité aminokyseliny sa budú pohybovať smerom ku katóde (-) a tie so záporným nábojom k anóde (+). Neutrálne nabité zlúčeniny, vyvážené kladnými a zápornými nábojmi v molekule, zostanú na rovnakom mieste.
Reakcie charakteristické pre karboxylovú skupinu
- Esterifikácia, ktorá spočíva v syntéze esterov produkovaných reakciou medzi aminokyselinou a alkoholom. Produkt takejto reakcie nevykazuje amfotérny charakter, ale vykazuje vlastnosti použitého amínu.
- Dekarboxylácia, to znamená zahrievanie aminokyseliny v prítomnosti roztoku hydroxidu bárnatého (Ba(OH) 2 ). Transformáciou vznikajú amíny.
- Tvorba komplexov súvisí so schopnosťou aminokyselín viazať sa s katiónmi kovu, najmä medi, čo spôsobuje tvorbu farebných zlúčenín (komplexných solí).

Reakcie charakteristické pre amínovú skupinu
- Deaminácia, ktorá sa týka aminokyselín, ktoré obsahujú primárnu aminoskupinu. Reakcia prebieha pod vplyvom kyseliny dusičnej (HNO 2 ) a aminokyselina použitá ako reaktant oxiduje a vytvára hydracidu. Amínová skupina sa uvoľňuje vo forme dusíka. Existuje niekoľko typov deaminácie, vrátane hydrolytickej deaminácie, hydrolytickej deaminácie s dekarboxyláciou, deaminácie redukciou a desaturačnej deaminácie.
- Oxidácia, ktorá spôsobuje premenu aminokyselín na ketokyseliny.
- Biochemické reakcie – všetky aminokyseliny, ktoré možno klasifikovať ako Schiffove zásady, sú schopné biochemických transformácií, ako je transmitancia a dekarboxylácia.
Reakcie používané na detekciu aminokyselín
- Ninhydrínová reakcia je farebná reakcia, kde reaktantmi sú aminokyselina a činidlo vo forme roztoku ninhydrínu. Reakciou vzniká charakteristická fialovo-modrá farba.
- Xantoproteínová reakcia je príkladom cesty k detekcii aromatických aminokyselín, ako je fenylalanín, tyrozín alebo tryptofán. Zlúčenina vystavená koncentrovanému roztoku kyseliny dusičnej ( HN03 ) zmení svoju farbu na žltú. Je výsledkom produkcie derivátov dusičnej aminokyseliny počas reakcie.
Zdroje aminokyselín
Aby sme zabezpečili dobrú fyzickú a psychickú kondíciu ľudského tela, mali by sme mu poskytnúť primerané množstvo každého stavebného materiálu, vrátane aminokyselín. Mimoriadne dôležitým zdrojom všetkých aminokyselín potrebných pre správne fungovanie sú kompletné bielkoviny. Zahŕňajú mäso, najmä hydinu, ryby, vajcia a mliečne výrobky. Mlieko obsahuje vysoké množstvo leucínu, izoleucínu, treonínu a tryptofánu. Lyzín a metionín možno nájsť v sóji. Valín môžeme dodávať spolu s ryžou, arašidmi, sezamom a mandľami, zatiaľ čo fenylalanínom zaradením vajec, syrov a obilných produktov do našej stravy. Prítomnosť aminokyselín v potravinách je bežná, ale aby bola naša strava správne vyvážená, produkty, ktoré používame, by mali byť diverzifikované. Obsahujú totiž len určité aminokyseliny zo skupiny nevyhnutných na udržanie správnych životných funkcií.





























































































































