Je to jedna ze dvou hlavních divizí analytické chemie, která se zabývá detekcí chemických prvků, funkčních skupin nebo iontů existujících v testované struktuře. Z hlediska použitých metod můžeme chemickou analýzu rozdělit na analýzu klasickou a analýzu instrumentální. Klasická analýza se opírá o metody založené na chemických reakcích, které mohou být prováděny v „suchém“ nebo „mokrém“ režimu. Naproti tomu instrumentální analýza spoléhá na přístroje, tedy analytické měřicí přístroje, jejichž hlavním prvkem je detektor.

Klasická analýza: suché reakce
Termín „suché reakce“ označuje změny, ke kterým dochází v chemických sloučeninách, když jsou vystaveny vysokým teplotám. Rozlišujeme tři hlavní typy takových reakcí:
- roztavení zkoušeného vzorku pevnými tavidly,
- získání boraxu nebo mikrokosmických solných kuliček,
- zbarvení plamene plynového hořáku.
Nejoblíbenější je třetí metoda, která se označuje jako plamenová zkouška a umožňuje detekovat mnoho prvků. Toto je příklad techniky, která využívá vyzařování záření. Spočívá ve zkoumání charakteristického záření, které vyzařují atomy jednotlivých prvků po jejich excitaci vysokou teplotou. To proto, že bylo prokázáno, že takové podmínky způsobují odpařování sloučenin určitých kovů a vznikající páry jsou excitovány a barví plamen hořáku charakteristickým způsobem. Barva je efektem excitace konkrétních atomů, které, když jsou navráceny do původního stavu, emitují světelné kvantum, které se vztahuje k určité vlnové délce. Například barvy plamene charakteristické pro jednotlivé prvky jsou následující:
- sodík: intenzivní žlutá,
- draslík: fialová,
- vápník: cihlově červený,
- baryum: zelená,
- vizmut: světle modrá.
Klasická analýza: mokré reakce
To jsou všechny typy reakcí, které se vyskytují mezi testovanými vzorky a roztoky různých chemických činidel . K provedení takových reakcí musí být testovaná látka převedena na roztok. Použité reakce jsou vybírány na základě mnoha kritérií tak, aby:
- vykazují vysokou citlivost, tj. vyskytují se již při nízkých koncentracích detekované látky;
- vyskytují se v krátkém čase a vykazují snadno pozorovatelné změny, jako je změna barvy roztoku, srážení nebo emise plynů;
- jsou selektivní, tj. vyskytují se pouze v rámci známé skupiny iontů.

Kvalitativní analýza: anorganická chemie
V anorganické chemii se kvalitativní analýza točí kolem dvou témat: detekce kationtů a aniontů. Anorganická chemie používá charakteristické reakce, které zahrnují vhodná skupinová činidla. Říká se jim „skupinová činidla“, protože kationty byly rozděleny do pěti kategorií. Takové činidlo tvoří sedimenty pouze s jedním z nich, což umožňuje zúžit typy kationtů přítomných ve vzorku podle následujícího vzorce:
- Skupina 1: Ag + , Hg 2 2+ , Pb 2+ – skupinové činidlo 3M HCl;
- Skupina 2: Hg 2+ , Cu 2+ , Cd 2+ , Bi 3+ , As 3+ , As 5+ , Sb 3+ , Sb 5+ , Sn 2+ , Sn 4+ – skupinové činidlo H 2 S v an prostředí 1M HCl;
- Skupina 3: Ni 2+ , Co 2+ , Fe 2+ , Fe 3+ , Mn 2+ , Zn 2+ , Al 3+ , Cr 3+ – skupinové činidlo (NH 4 ) 2 S v prostředí amonného pufru;
- Skupina 4: Ca 2+ , Sr 2+ , Ba 2+ – skupinové činidlo (NH 4 ) 2 CO 3 v prostředí amoniového pufru;
- Skupina 5: Mg2 + , Na + , K + , NH4 + – žádné skupinové činidlo.
Jakmile vyloučíme určité skupiny kationtů, můžeme pokračovat v identifikaci s použitím dalších činidel, tentokrát charakteristických pro jednotlivé ionty. Taková reakce umožňuje jednoznačnou identifikaci. Například detekce iontů Ag + ve vzorku probíhá ve dvou fázích:
- Reakce se skupinovým činidlem: tvorba bílého sedimentu
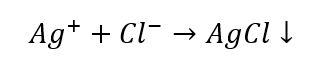
- Charakteristická reakce: rozpuštění sedimentu AgCl ve vodném roztoku amoniaku, získání bezbarvé komplexní sloučeniny.
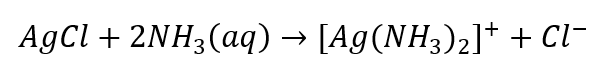
Podobným způsobem můžeme identifikovat anionty, které se dělí do tří skupin:
- Skupina 1 : BO2- , CO32- , C2042- , Si032- , PO43- , AsO33- , As043- , SO32- , S2032- , SO 4 2- , F – , CrO 4 2- , Cr 2 O 7 2- – skupinové činidlo BaCl 2 , tvorba solí těžko rozpustných ve vodě;
- Skupina 2: C 4 H 4 O 6 2- , S 2- , Cl – , ClO – , Br – , I – , CN – , SCN – – skupinové činidlo AgNO 3 , tvorba solí těžce rozpustných ve vodě a v řed. kyselina dusičná;
- Skupina 3: CH 3 COO – , NO 2 – , NO 3 2- , ClO 3 – , ClO 4 – , MnO 4 – – skupinové činidlo obsahuje kationty stříbra nebo barya; tvorba ve vodě rozpustných solí.
Identifikace kationtů je ve srovnání s anionty poněkud problematičtější, protože sled postupů závisí na výsledcích skupinových reakcí a navíc existují ionty, které narušují proces identifikace. Například pro detekci iontu CO 3 2- musíme provést následující reakce:
- Ionty Ba 2+ vytvářejí bílý sediment, který je rozpustný v kyselinách
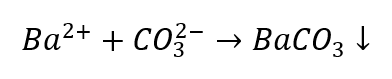
- Zředěné kyseliny způsobují rozklad srážením CO 2
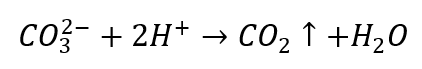
- Oxid uhličitý způsobuje bublání roztoku. Může být pokryta vápennou vodou, protože se vysráží bílý sediment.
* Rušivé ionty: SO 3 2- a S 2 O 3 2- tvoří s kationtem vápníku také bílé sedimenty. Musí být oxidovány, aby se rušení odstranilo. 
Kvalitativní analýza: organická chemie
Kvalitativní analýza organických sloučenin zahrnuje několik fází a klíčovým bodem je vyřešit pět základních problémů:
- Stanovení fyzikálních parametrů , jako je bod tání nebo bod varu. Bohužel existuje mnoho chemických sloučenin se stejnými teplotními body a samotné měření může být ovlivněno chybou. Pokud však máme vhodný referenční standard, může nám tato metoda umožnit rychlou identifikaci sloučeniny. Navíc měřením teplot můžeme určit čistotu sloučeniny, protože teplotní rozsahy jsou úzké. Stálost T top po alespoň jedné krystalizaci může také naznačovat vysokou čistotu sloučeniny. U kapalin může znamenat úzký destilační rozsah.
- Stanovení elementárního složení může vyloučit nebo potvrdit přítomnost konkrétních typů organických sloučenin. Abychom uvedli příklad, vyloučením přítomnosti atomů dusíku ve struktuře také vylučujeme přítomnost amino nebo dusičnanových skupin. Za tímto účelem provádíme charakteristické experimenty, jako je Lassaigneův test na dusík, Beilsteinův test na halogeny nebo sírový test s nitroprusidem sodným.
- Testování rozpustnosti sloučeniny umožňuje zařadit ji do skupiny sloučenin se stanovenými chemickými vlastnostmi. Podle principu „podobné se rozpouští jako“ byly sloučeniny rozděleny do 7 kategorií.
- Identifikace funkčních skupin vyžaduje vhodné analytické reakce, které umožňují vyloučit nebo identifikovat funkční skupiny.
- Spektrální analýza je nejspolehlivějším bodem, který nám umožňuje jasně identifikovat chemickou sloučeninu. Zahrnuje všechny instrumentální techniky, jako např.
- Hmotnostní spektrometrie (MS) , která spočívá v ionizaci molekul a detekci počtu iontů stanovením jejich poměru hmotnosti k náboji. To nám umožňuje vyvodit závěry o hmotnosti analyzované sloučeniny;
- Spektroskopie nukleární magnetické rezonance (NMR) , která poskytuje specifické informace o struktuře. Poskytuje obraz magnetických jader ( 13 C, 1 H), což umožňuje důkladnou interpretaci jejich kvality;
- Infračervená (IR) spektroskopie využívá úzký rozsah elektromagnetického záření k zobrazení typů vibrací existujících v testované molekule.





























































































































