L'indice HLB ( équilibre hydrophile-lipophile ) est également appelé équilibre hydrophile-lipophile ou équilibre hydrophobe. Il s'agit d'une échelle de valeurs représentant le rapport entre les parties hydrophiles et lipophiles d'une molécule. Ce paramètre permet de déterminer le degré de polarité des composés chimiques. L'intérêt de la mesure du HLB d'une molécule est le plus souvent abordé dans le contexte des émulsifiants, c'est-à-dire une famille de tensioactifs.

Échelle HLB
Il s’agit d’une échelle conventionnelle, la première de l’histoire, appelée échelle de Griffin , qui comporte vingt degrés, de 0 à 20, et qui se rapporte principalement aux tensioactifs non ioniques . La position des propriétés d’une substance sur l’échelle permet de prédire certaines caractéristiques :
- On suppose que, de zéro à dix, une substance a une plus grande affinité pour les molécules lipophiles et se dissout donc mieux dans les huiles et les composés hydrophobes que dans l’eau.
- Au-delà de dix, l’affinité pour l’eau et les particules hydrophiles augmente. Les tensioactifs dont l’indice HLB est supérieur à 10 sont donc plus hydrophiles ; leur solubilité augmente dans l’eau et diminue dans les huiles.
- Une valeur intermédiaire de 10 indique que le composé possède à la fois des parties hydrophiles et hydrophobes. Le rapport entre leurs valeurs est approximativement de 1:1.
- Valeurs extrêmes : 0 indique un composé constitué exclusivement de groupes hydrophobes, et 20 est attribué aux substances qui ne possèdent que des parties hydrophiles dans leur structure.
Que nous apprend l’échelle HLB ?
Dans le contexte de l’utilisation des tensioactifs , l’équilibre hydrophile-hydrophobe est fondamental pour le développement des formulations. Selon sa valeur, les tensioactifs possèdent différentes propriétés :
- Valeurs de 1 à 3 – agents anti-mousse ,
- Valeurs de 3 à 6 – Émulsifiants E/H (eau dans huile), donnant l’effet d’une suspension laiteuse,
- Valeurs de 7 à 9 – agents mouillants et enrobants, qui constituent une suspension laiteuse stable,
- Valeurs de 9 à 18 – Émulsifiants H/E, c’est-à-dire huile dans eau, qui sont pour la plupart des suspensions transparentes et limpides,
- Valeurs de 13 à 15 – agents de lavage, détergents , solutions transparentes,
- Valeurs de 13 à 18 – solubilisants , solutions transparentes.
La connaissance de la valeur HLB permet, entre autres, de sélectionner l’ émulsifiant adapté à un système d’émulsion donné.
Extension de l’échelle de Griffin
L’échelle initiale de 20 points a finalement été étendue à 40 points. Ceci est dû aux composés lipophiles ioniques, qui deviennent de plus en plus hydrophiles lors des changements de solution.
Comment calculer le HLB ?
- Pour la plupart des substances, nous utilisons une formule simplifiée :
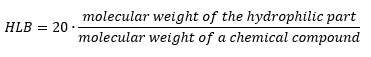
- Pour les acides gras oxyéthylés, c’est-à-dire les composés du groupe ester, une formule a été établie, étendue par leurs indices de saponification et d’acide.
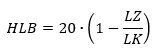
Où:
- LZ – indice de saponification du produit d’oxyéthylation
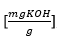 ,
, - LK – indice d’acide de l’acide oxyéthylé
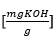 .
.
Méthodes expérimentales
L’indice HLB peut non seulement être calculé, mais aussi déterminé et vérifié expérimentalement. Ceci est réalisé grâce à des techniques telles que les méthodes d’émulsion, la spectrophotométrie RMN et la chromatographie en phase gazeuse, qui reposent sur les propriétés caractéristiques des tensioactifs, notamment :
- Chaleur d’adsorption,
- Propriétés moussantes,
- angle de mouillage,
- Tension interfaciale,
- CMC, ou concentration micellaire critique ,
- PIT, ou température d’inversion de phase.

Émulsions
L’équilibre hydrophile-hydrophobe est un élément clé dans le choix des formulations fonctionnelles. Toute émulsion, par exemple les crèmes, les lotions et les baumes, est composée de deux phases : une phase aqueuse et une phase huileuse. Du fait de leurs propriétés chimiques différentes, ces deux phases ne se mélangent pas et, lorsqu’on tente de les homogénéiser, elles ne forment que des émulsions instables. Les molécules de l’une sont dispersées ou en suspension entre les molécules de l’autre. C’est pourquoi des substances appelées émulsifiants sont ajoutées aux formulations afin d’améliorer la capacité des autres ingrédients à former des émulsions stables.
Quels sont les critères qui déterminent le choix de l’émulsifiant idéal ?
-
- Propriétés et composition de la phase lipidique,
- Type d’émulsion souhaité :
- Une émulsion H/E (huile dans eau) est un type d’émulsion couramment utilisé en cosmétique, dans laquelle la phase huileuse lipophile est dispersée dans la phase aqueuse hydrophile. Ces émulsions se caractérisent par une consistance légère et une absorption facile.
- Une émulsion E/H (eau dans huile) est une émulsion dans laquelle la phase aqueuse hydrophile est dispersée dans la phase huileuse lipophile. Ces émulsions se caractérisent par une consistance plus grasse et plus dense, ce qui contribue à limiter la déshydratation et à protéger la peau des agressions extérieures.
Exemples d’émulsifiants eau/huile
Émulsifiants non ioniques, qui sont des esters d’alcools et d’acides gras, des esters d’alcools polyhydriques et d’acides gras, des esters de sorbitan et d’acides gras supérieurs :
-
-
- Cire d’abeille blanche,
- Cire d’abeille jaune,
- Lanolin,
- Monostéarate de glycéryle.
-
Exemples d’émulsifiants H/E
Ce groupe comprend les émulsifiants anioniques et non ioniques :
-
-
- Savons : sels de sodium, de potassium et d’ammonium d’acides gras supérieurs et savons de métaux multivalents, tels que l’oléate de magnésium,
- Polysorbates : Tween, Myrj, polymères séquencés.
-
HLB en pratique
Pour les matières premières grasses, nous pouvons établir une liste des meilleurs émulsifiants, en fonction du type d’émulsion souhaité. Voici des exemples d’émulsifiants HLB utilisables pour obtenir une émulsion à partir d’une matière première donnée et d’eau : Composant de la phase lipophile pour émulsions
| Ingrédient de phase lipophile pour émulsions | Sans | O/W |
| acide stéarique | 6 | 15 |
| Cetyl alcohol | – | 15 |
| alcool stéarylique | – | 14 |
| lanoline anhydre | 8 | 10 |
| Huile de coton | 5 | 10 |
| Huile minérale | 5 | 12 |
| Cire d’abeille | 4 | 12 |
Exemple : Pour obtenir une émulsion eau dans huile (E/H) à base de cire d’abeille et d’eau, il convient d’utiliser un émulsifiant ayant un HLB de 4. Pour obtenir une émulsion huile dans eau (H/E) à partir des mêmes ingrédients, il est nécessaire d’utiliser un émulsifiant ayant un HLB de 12. Dans le cas de l’alcool cétylique et de l’alcool stéarylique, la production d’une émulsion E/H ne nécessite pas la présence d’un émulsifiant.
Calcul du HLB d’un émulsifiant
Afin de stabiliser l’émulsion souhaitée, il est nécessaire de calculer l’indice HLB de l’émulsifiant ou du mélange d’émulsifiants. Dans ce cas, l’indice HLB est calculé uniquement pour la phase grasse, même si sa proportion dans la formulation est négligeable. Pour les mélanges d’émulsifiants, l’indice HLB est calculé en fonction des composants individuels et de leurs proportions relatives. La plupart des huiles, beurres et cires ont un indice HLB compris entre 6 et 8, mais certaines graisses peuvent s’en écarter significativement. Par exemple, l’indice HLB de l’huile de ricin est de 14. Cela signifie que l’utilisation d’un mélange de graisses dans la phase huileuse peut entraîner une modification importante de l’indice HLB de l’émulsifiant recommandé, en fonction des proportions de ses composants.
Exemples de valeurs HLB pour les émulsifiants
-
- GMS : 3-4,
- Monostéarate de propylène glycol : 3,4,
- Monostéarate de glycérol : 3,8,
- Portée 80 : 4,3,
- Tween 80 : 15,
- Polysorbate 20 : 16-17.
- Michocka, K. Otrzymywanie i właściwości użytkowe nowych surfaktantów z ugrupowaniem cukrowym. Uniwersytet Ekonomiczny w Poznaniu, 2012. Wydawnictwo UE Poznań – wersja podglądowa PDF dostępna online: https://wydawnictwo.ue.poznan.pl/books/978-83-8211-090-6/sample.pdf
- Receptura.pl. „Równowaga hydrofilowo-lipofilowa i jej znaczenie w recepturze aptecznej.” Dostęp online: https://receptura.pl/rownowaga-hydrofilowo-lipofilowa-i-jej-znaczenie-w-recepturze-aptecznej/
- Zgoda, M. M., Hreczuch, W., Woskowicz, M., Nachajski, M., Kołodziejczyk, M. „Związki powierzchniowo czynne z grupy polioksyetylenowanych estrów kwasów tłuszczowych.” Polimery, 2003.































































































































